חזית המחקר
השפעת רצף של בצורות בצפון הנגב על תכונות הקרקע ועל תמותת הצומח
יוני שיר המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגב
זאב רונן המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגב
עלי נג'ידאת המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגב ([email protected])

בצורות ממושכות מביאות לתמותה נרחבת של צומח | צילום: ענב וידן
מאת
אלי צעדי
המחלקה למשאבי טבע וגד"ש, ִמנהל המחקר החקלאי, מרכז מחקר גילתיוני שיר
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבזאב רונן
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבעלי נג'ידאת
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבמאת
אלי צעדי
המחלקה למשאבי טבע וגד"ש, ִמנהל המחקר החקלאי, מרכז מחקר גילתיוני שיר
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבזאב רונן
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבעלי נג'ידאת
המחלקה להידרולוגיה ומיקרוביולוגיה של הסביבה, המכון ע"ש צוקרברג לחקר המים, המכונים לחקר המדבר ע"ש בלאושטיין, אוניברסיטת בן-גוריון בנגבבמערכות אקולוגיות מדבריות, אירועי הגשם קובעים את קצב פירוק החומר האורגני ואת מחזורי הנוטריינטים. כתמי הצומח קובעים את המקומות שמתקיימים בהם קצבים גבוהים יותר של פעילויות ביוגאוכימיות לעומת אלה שבשטחי הקרקע שביניהם. במערכות אלה, זמינות החנקן היא הגורם השני בחשיבותו, לאחר המים, המגביל את ייצור הביומסה הצמחית. בעשור האחרון חלה בצפון הנגב ירידה בכמות הגשמים שהסתיימה ברצף של ארבע שנות בצורת. בשנים האחרונות נצפתה תמותה נרחבת של חלק ממיני השיחים השולטים באזור, שהביאה אותנו לשער כי הדבר יבוא לידי ביטוי באופן מובהק במחזור הנוטריינטים בקרקע. המחקר הנוכחי בדק את השינויים בתכונות הכימיות של הקרקע, ובמיוחד ברמות החנקן האי-אורגני. מתחנת המחקר האקולוגי ארוך הטווח בפארק סיירת שקד בצפון הנגב נאספו דגימות של קרקע מתחת לחופה של שיחים חיים ומתים של נואית קוצנית ומתנן שעיר. השינוי העיקרי שחל בעונה לאחר תמותת השיחים (2009) היה העלייה בריכוזי חנקה (ניטרט) בכל הדוגמאות. פעילותם של מיקרואורגניזמים מחמצני אמוניום שנמדדה בחורף שלאחר תמותת השיחים הייתה גבוהה יותר בקרקעות מתחת לשיחים המתים. ככל הנראה, אירועי גשם, המתקיימים גם כאשר הכמות השנתית הממוצעת של הגשם נמוכה יחסית, מייצרים את לחות הקרקע הדרושה לפעילות המיקרואורגניזמים. אנליזות בשיטות ביו-מולקולריות לא הראו שינויים משמעותיים במבנה האוכלוסיות של המיקרואורגניזמים מחמצני האמוניום בקרקעות שמתחת לשני מיני השיחים, דבר המצביע על עמידותם לעלייה ברמת הצחיחות שחלה באזור. ניתן להסיק כי היעלמות השיחים בעקבות הבצורת באזור היבש של צפון הנגב לא השפיעה על מבנה אוכלוסיות מחמצני האמוניום אך גרמה להצטברות החנקה. הצטברות החנקה היא תוצאה של ייצור אמוניום (קיבוע על-ידי מיקרואורגניזמים עמידים ליובש, הפרשות של שבלולים ופירוק של חומר אורגני) וחמצונו לחנקה על-ידי ניטריפיקנטים עמידים ליובש וכן של היעדר הצרכנים (שיחים). החנקות שנוצרו עלולות מחד גיסא להישטף לעומק הקרקע, ומאידך גיסא לנוע עם הנגר ולזהם מאגרי מים במורד. כמו כן, הן עלולות לשמש מקור לגזי חממה בתהליכי דה-ניטריפיקציה.
על קצה המזלג
סיכום ומשמעויות
המאמר עוסק בתהליכים המתקיימים במערכות אקולוגיות באזורי מדבר בעקבות שנים רצופות של בצורת, ובפרט בשינויים במחזור החנקן בקרקעות צפון הנגב. כל תהליכי החיים בצמח ובקרקע מתרחשים בנוכחות מים ובאמצעותם – בהיעדרם עלול הצמח להיפגע. כמויות מים נמוכות מהרגיל, לאורך מספר שנים רצופות, גורמות ככל הנראה לנזקים מצטברים בשיחים, ובסופו של דבר למותם. גם החנקן הוא מרכיב חשוב בצמח ובהיעדרו מפסיק הצמח לצמוח ולבסוף מת.
במחקר נמצא שכמות החנקה (מקור חנקן זמין לצמחים) תחת שיחי מתנן שעיר שמתו, גבוהה מזו הקיימת תחת שיחי מתנן חיים. עובדה זו מעידה על פעילות של המיקרואורגניזמים האחראים ליצירת החנקה בקרקע, למרות המגבלה בכמות המים. כמות החנקה הגבוהה מתחת לשיחים המתים נובעת ככל הנראה מכמות גדולה יחסית של החנקן הכללי בקרקע, שמקורו בחומר האורגני של השיח המת, ומכך שבמות השיח אין מי שינצל את החנקה. הימשכות הבצורות עשויה לגרום לדעיכת קצב יצירת החנקה בקרקע, בהיעדר אספקת חנקן כללי מהצומח.
משמעויות אפשריות של המחקר הן שבמקרה שרצף הבצורות יימשך או יהיה חלק מתהליך של שינוי האקלים באזור, אזי "עודפי החנקה" יישטפו מהקרקע ויזהמו את מקורות המים. כמו כן, עודפי חנקה עלולים לתרום לזיהום האוויר כתוצאה מתהליך הדה-ניטריפיקציה של החנקה. למסקנות אלו יש להתייחס בזהירות, מכיוון שכמויות החנקה המשתחררות משטחים חקלאיים גדולות הרבה יותר מאלו שהתקבלו במחקר זה, ומשום שמספר שנות בצורת מעידות על תנודות במשקעים באזור ולא על שינוי אקלים המתרחש בטווחי זמן ארוכים מאוד.
המערכת
הלכה למעשה
מבוא
האזורים הצחיחים מכסים כ-40% מהמערכות היבשתיות על פני כדור הארץ. אזורים אלה מאופיינים במאזן מים שלילי של משקעים ובהתאדות גבוהה [32]. מערכות אקולוגיות צחיחות נחשבות פגיעות יותר לשינויים קיצוניים במשטרי האקלים, שעלולים להאיץ תהליכי מדבור ולפגוע במגוון האקולוגי, בשירותי המערכת וברווחת בני האדם המאכלסים אזורים אלה [30].
שינוי האקלים הגלובלי מורגש בעוצמה רבה באזורים צחיחים ומתבטא בעלייה בטמפרטורה השנתית הממוצעת של הקרקע, בירידה בכמות המשקעים הממוצעת ובשינויים במספר אירועי הגשם ובעוצמתם [9]. לשינויים אלה יכולה להיות השפעה משמעותית על הקיימות של מערכות אקולוגיות כתוצאה משינויים במגוון הביולוגי ובקצב הפעילויות הביולוגיות המתלוות לכך [28]. נוסף על כך, שינויים שחלים במגוון הביולוגי של המערכת האקולוגית יכולים בתורם לגרום לשינויים בשירותים שמערכת זו מספקת לסביבתה [30]. בכל המערכות היבשתיות, המחזורים הביוגאוכימיים בקרקע מהווים את הבסיס לשירותים אלה, מאחר שהם מספקים את הנוטריינטים הדרושים לרמת הייצור, לזרימות ולתנועת האנרגיה אל המערכת האקולוגית ומחוצה לה [4, 26].
הנוף של צפון הנגב מאופיין בכתמי שיחים שביניהם מרווחים של קרקע, שמכוסים בדרך כלל בקרום ביולוגי [1]. נמצא, כי כתמי השיחים הם מרכזים לפעילויות ביוגאוכימיות בקצבים גבוהים [7, 23, 37], ויוצרים איים של פוריות בנוף. אירועי הגשם בתחילת החורף, כמותם ואורכם, הם אלה הקובעים את מועדי הפירוק של החומר האורגני ואת מחזורי הנוטריינטים [3, 37]. על כן, השינויים במשטר הגשמים, באוכלוסיות ובכיסוי הצומח יכולים להשפיע באופן מובהק על המעגלים הביוגאוכימיים בקרקעות מדבריות ובכך על תהליכי המדבור [32].
החנקן נחשב כגורם המגביל השני בחשיבותו לאחר המים לייצור הראשוני, ולכן במערכות צחיחות מצביעה זמינותו על היצרנות של המערכת האקולוגית [31, 33]. מחזור החנקן, כמו מחזורים ביוגאוכימיים אחרים במערכות צחיחות, יכול להיות מושפע משינויים סביבתיים בעקבות שינוי האקלים הגלובלי [3]. עם העלייה ברמת הצחיחות ישנה נטייה להצטברות של תרכובות חנקן אי-אורגני בקרקע [5]. חנקן זה, בעיקר החנקה (ניטרט, –NO3], יכול בקלות להישטף לעומק, לנוע בנגר העילי ולזהם מאגרי מים סמוכים או לתרום להצטברות גזי חממה באטמוספרה [3].
שינויים בכיסוי הצומח יכולים לנבוע ממספר סיבות, כגון פלישה נרחבת של מינים פולשים, שרֵפות, רעייה כבדה וסיבות אחרות [19]. גם שינוי האקלים הגלובלי הוכח כבעל השפעה על אוכלוסיות הצומח, בייחוד במערכות אקולוגיות צחיחות. שינויים אלה גורמים לתקופות ממושכות של בצורת המביאה לתמותה רחבת היקף של הצומח המעוצה [2].
בארבע השנים האחרונות מאובחן רצף של בצורות בצפון הנגב, מממוצע של כ-150 מ"מ משקעים בשנה לפחות מ-100 מ"מ (איור 1). תופעה זו הביאה לתמותה נרחבת של שיחים. אנו משערים כי שינוי זה מתבטא בתכונות הכימיות של הקרקע ובייחוד בטרנספורמציה של החנקן.
מטרת מחקר זה היא לקשר בין התמותה הנרחבת של השיחים הדומיננטיים לבין השינויים בתכונות הכימיות של הקרקע ובפרט השינויים במחזור החנקן.
שיטות
אתר המחקר ודגימת הקרקע – דגימות הקרקע נאספו בתחנת המחקר האקולוגי ארוך הטווח (LTER) בפארק סיירת שקד שבצפון הנגב (31º17'N; 34º37'E). בעשרים השנים האחרונות ירדו באזור זה בממוצע כ-150 מ"מ גשם. טמפרטורת המינימום 6–8 מעלות צלזיוס בחורף ו-32–34 מעלות בקיץ. דגימות הקרקע נאספו במרץ 2008, באפריל 2009 – לאחר אירוע התמותה הנרחב של השיחים – ובמרץ 2010. דגימות הקרקע (עד לעומק של 10 ס"מ) נאספו מתחת לחופה של שלושה שיחים חיים ומתים של נואית קוצנית (Noaea mucronata), שלושה שיחים חיים ומתים של מִתנן שעיר (Thymelaea hirsute) וכן מאזור הכתמים שמכוסים בקרומים ביולוגיים שבין השיחים. הדוגמאות נאספו לתוך שקיות פוליאתילן סטריליות, בתוך קרח, הובאו למעבדה תוך 90 דקות מהאיסוף, והיו מוכנות לאנליזות כפי שיפורט בהמשך.
בדיקות כימיות של הקרקע – דגימות הקרקע עברו ניפוי (2.0 מ"מ להרחקת אבנים וחלקי צמחים) ויובשו בתנור ב-65 מעלות במשך 24 שעות. תרכובות חנקן מינרליות משלביו השונים של מחזור החנקן (אמוניום, +NH4 ), חנקית (ניטריט, –NH2) וחנקה מוצו לאחר טלטול במשך 60 דקות באשלגן כלוריד (10 גרם קרקע ב-40 מ"ל תמיסת 1M KCl) בטמפרטורת החדר וסוננו (Whatman No. 1). תכולת האמוניום הכללית (TAN) נקבעה לפי שיטת Nessler, החנקִית בסולפונילאמיד [8] והחנקה לפי שיטת Ferree ו-[10] Shannon. תכולת המים (WC) נקבעה בשיטה הגרווימטרית בדוגמאות ההתחלתיות לאחר ייבוש ב-105 מעלות. ערך ההגבה (pH) והמוליכות החשמלית (מדד למליחות הקרקע לפי המוליכות החשמלית, Electrical conductivity [EC]) נמדדו במד-מוליכות ובמד ערך הגבה (pH meter) במיצוי קרקע (1:1) במים מזוקקים. החומר האורגני הכולל נקבע בדגימות שעברו ייבוש בתנור ב-105 מעלות בשיטת השרֵפה בכבשן (450 מעלות במשך 8 שעות, לאחר שטיפה בחומצה חלשה) [6].
פוטנציאל חמצון האמוניום (AOP) – מדד להשוואה של פעילות החנקון (ניטריפקציה – חמצון אמוניום לחנקה – (AOP בין דוגמאות הקרקע השונות. נקבע על-ידי שיטה שמודדת את פעילות חמצון האמוניום. בשיטה זו עוקבים אחר הצטברות החנקית במצע המכיל 2(NH4), K2HPO4, ו-KClO3, מעכב מחמצני חנקית, תוך טלטול במשך 6 שעות [18].
מיצוי די אן איי וקביעת מספר העותקים של גנים – הדי-אן-איי הגנומי מוצה מהקרקע בעזרת PowerSoil™ DNA Isolation Kit. מדידת מספר העותקים של הגן (amoA), המקודד לאנזים אמוניום-מונו-אוקסיגינאז כמדד למספר החיידקים המעורבים בחִמצון אמוניום, נעשה בשיטת ה-Q-PCR. בשיטה זו, כמות העותקים של גן מסוים נמדדת לפי מספר המחזורים של תגובות ה-PCR עד שניתן להבחין בהצטברות משמעותית של אותו גן בעקבות יצירת מספר גדול של עותקים. מספר המחזורים תלוי בכמות ההתחלתית של הגן [24].
האנזים מעורב בחמצון אמוניום לחנקית, וחמצון זה נחשב כשלב הראשון והמגביל בתהליך החנקון. חמצון זה מתבצע על-ידי שתי קבוצות מיקרואורגניזמים – בקטריה וארכֵאה. הערכות כמותיות של מחמצני אמוניום בקטריאליים וארכֵאליים בקרקעות שנדגמו, נעשו על-ידי כימות הגן amoA הבקטריאלי והארכֵאלי. מספר העותקים של הגן השייך לקבוצת הבקטריות נעשה לפי התנאים המפורטים ב-Rotthauwe ועמיתיו [21], ואילו מספר העותקים של הגן השייך לקבוצת הארכֵאות נעשה לפי התנאים המפורטים ב-Francis ועמיתיו [21]. הבדיקות נעשו במכשיר Rotor Gene™ 6000.
סטטיסטיקה – נעשה שימוש בתוכנת סטטיסטיקה לניתוח ANOVA, ובמבחני Tukey HSD post hoc.

תוצאות
בעקבות התמעטות הגשמים, בייחוד בארבע השנים האחרונות, אירעה בקיץ 2008 תמותה נרחבת של שיחי נואית קוצנית ומתנן שעיר בצפון הנגב (איור 2). מאחר שאתר המחקר (פארק סיירת שקד) משמש תחנת מחקר אקולוגית ארוכת טווח, היו בידינו תוצאות של בדיקות קרקע עוד לפני אירוע התמותה הנרחב בקיץ 2009. דבר זה נתן בידינו את האפשרות להשוות בין התכונות הכימיות של הקרקע לפני התמותה ולאחריה.
איור 2
שיחי נואית קוצנית ומתנן שעיר חיים (א ו-ב, בהתאמה) ומתים (א1 ו-ב1, בהתאמה) לאחר שנפגעו מרצף הבצורות. השטח לאחר היעלמות השיחים, ובו כתמים לבנים של שבלולים מתים שחיו על ענפי השיחים (ג).
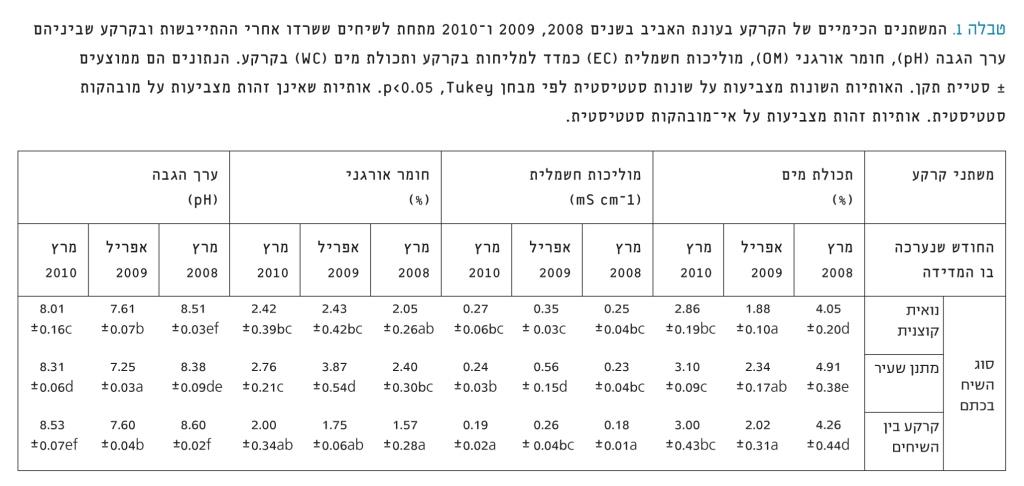
מאפיינים כימיים של הקרקע – ניתוח של דגימות הקרקע שנאספו במשך שלוש שנים רצופות הצביע על שינויים משמעותיים במשתנים הכימיים של הקרקע שחלו בשנה הראשונה לאחר תמותת השיחים. המליחות (המוליכות החשמלית, EC) עלתה באופן משמעותי בדגימות הקרקע שנאספו מתחת לשיחי המִתנן השעיר ששרדו ובקרקע שבין השיחים. העלייה במליחות, לאחר התמותה, הייתה מתונה יותר בקרקע שמתחת לצמחי הנואית הקוצנית (טבלה 1). ערכי ההגבה (טבלה 1) בכל הדוגמאות ירדו באופן משמעותי בשנה הראשונה, לאחר תמותת השיחים, אך עלו בחזרה בשנה שלאחריה (2010). נוסף על כך, כמות החומר האורגני שהצטבר מתחת לשיחי המתנן ששרדו עלתה ב-60% בשנה הראשונה לאחר תמותת השיחים (טבלה 1).
בדגימה של 2009 נעשתה השוואה בין המשתנים הכימיים של דגימות קרקע שנאספו מתחת לשיחים ששרדו לבין אלה שנאספו מתחת לצמחים מתים. התוצאות הראו ריכוזי חנקה גבוהים יותר (p<0.05) בדגימות שנאספו מתחת לשיחים המתים של הנואית הקוצנית (21.1 מיליגרם חנקן לק"ג קרקע) לעומת אלה שנאספו מתחת לשיחים החיים (8.93 מיליגרם חנקן לק"ג קרקע). הערכים בדגימות הקרקע של שיחי המתנן השעיר המתים והחיים היו 23.62 ו-13.51 מיליגרם חנקן לק"ג קרקע, בהתאמה. לעומת זאת, לא נמצאו הבדלים בערכי ההגבה והמליחות בין דגימות הקרקע (2009) שנאספו מתחת לשיחים חיים לעומת אלה שנאספו מתחת לצמחים המתים. ריכוזי האמוניום היו 13.29 ו-7.50 מיליגרם חנקן לק"ג בקרקעות שנאספו מתחת לשיחי נואית קוצנית מתים לעומת אלה שנאספו מתחת לשיחים חיים, בהתאמה.
טבלה 1
המשתנים הכימיים של הקרקע בעונת האביב בשנים 2008, 2009 ו-2010 מתחת לשיחים ששרדו אחרי ההתייבשות ובקרקע שביניהם
ערך הגבה (pH), חומר אורגני (OM), מוליכות חשמלית (EC) כמדד למליחות בקרקע ותכולת מים (WC) בקרקע. הנתונים הם ממוצעים ± סטיית תקן. האותיות השונות מצביעות על שונות סטטיסטית לפי מבחן p<0.05 ,Tukey. אותיות שאינן זהות מצביעות על מובהקות סטטיסטית. אותיות זהות מצביעות על אי-מובהקות סטטיסטית.
ככלל רמות החומר האורגני היו 3.5% ו-2.4% בקרקעות של שיחים מתים וחיים, בהתאמה. בקרקעות שתחת שיחים מתים של מתנן שעיר נמצאו ריכוזי אמוניום נמוכים יותר מאלה של קרקעות מתחת לשיחים החיים (15.1 ו-8.7 מיליגרם חנקן לק"ג קרקע, בהתאמה).
פעילות ומבנה אוכלוסיות מחמצני האמוניום – בדגימה של השנה הראשונה שלאחר תמותת השיחים, נמצא פוטנציאל חמצון אמוניום (AOP) נמוך בקרקעות מתחת לשיחים ששרדו לעומת אלה מתחת לשיחים המתים. בשנה השנייה שלאחר התמותה, פוטנציאל חִמצון האמוניום היה הגבוה ביותר מתחת לשיחים של נואית קוצנית. מבנה אוכלוסיות מחמצני האמוניום (בקטריה וארכֵאה) נבדק בשיטת מפל הצמיתה (denaturation) והרצה בג'ל [17] (DGGE) ולא נמצאו הבדלים במבנה האוכלוסיות מחמצני האמוניום (בקטריה וארכֵאה) בין הדגימות שנאספו מתחת לשיחים החיים והמתים. כמו כן, לא נמצאו הבדלים בין דגימות הקרקע שנאספו לפני תמותת השיחים ולאחריה (התוצאות לא מוצגות). בחורף הראשון שלאחר תמותת השיחים, היה מספר העותקים של הגן amoA של הארכֵאה 1.37X108 עותקים לגרם קרקע בממוצע, וירד ל-1.36X107 בחורף שלאחר מכן. מספר העותקים של הגן amoA של הבקטריה, לעומת זאת, עלה מ-6.25X106 עותקים לגרם קרקע ל-2.47X107 בחורף שלאחר מכן (טבלה 2). הבדלים משמעותיים לגבי שכיחות המינים של מחמצני האמוניום נמצאו מתחת לשיחים מתים של מתנן שעיר לעומת החיים (8.54X107 ו-1.12X107 עותקים לגרם קרקע, בהתאמה) (טבלה 2).
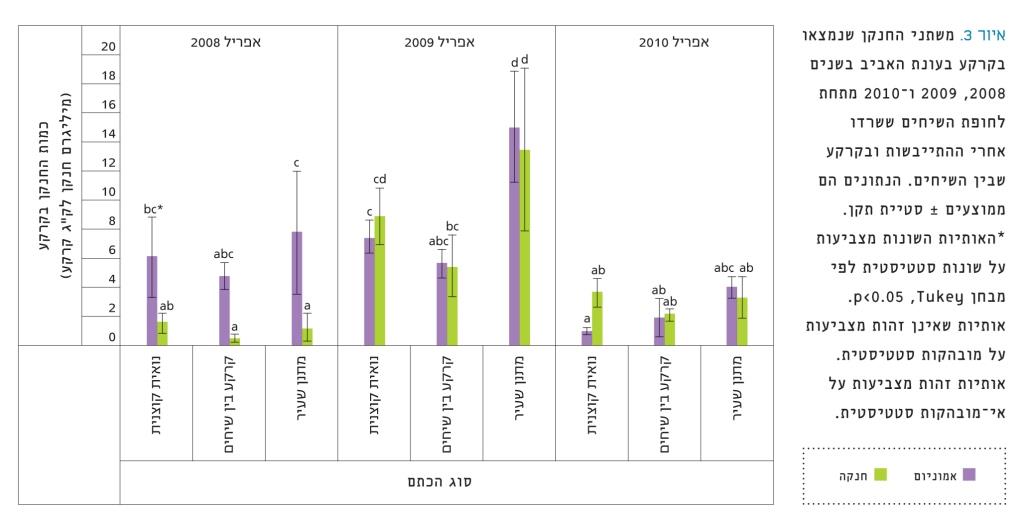
איור 3
משתני החנקן שנמצאו בקרקע בעונת האביב בשנים 2008, 2009 ו-2010 מתחת לחופת השיחים ששרדו אחרי ההתייבשות ובקרקע שבין השיחים
הנתונים הם ממוצעים ± סטיית תקן.
*האותיות השונות מצביעות על שונות סטטיסטית לפי מבחן p<0.05 ,Tukey. אותיות שאינן זהות מצביעות על מובהקות סטטיסטית. אותיות זהות מצביעות על אי-מובהקות סטטיסטית.
דיון
מחקר זה מתאר את השפעת השינויים, שחלו בכיסוי צמחיית השיחים בעקבות רצף של שנות הבצורת, על מחזור החנקן במערכת אקולוגית באזור צחיח למחצה. שינוי אקלים יכול לגרום שינויים במאפייני הקרקעות על-ידי שינויים בכמויות הגשמים [35]. מחקר זה הראה כי הרצף של ארבע שנות הבצורת הביא לתמותה משמעותית של מיני השיחים. בשנה הראשונה לאחר התמותה (2009) הייתה עלייה במליחות הקרקע וירידה בערכי ההגבה (טבלה 1). השינויים השנתיים הללו בערכי ההגבה ובמליחות הקרקע יכולים להשפיע בהמשך על הפעילות הביולוגית, למשל על הפירוק של החומר האורגני ועל מחזור החנקן. Groffman ו-Tiedje [13] הראו כי ירידה בתכולת המים בקרקע מאטה את קצב הדה-ניטריפיקציה, מאחר שכתוצאה מכך יש פחות בתי גידול אל-אווירניים (unaerobic). תופעה זו יכולה לתרום להצטברות של חנקה בקרקע על אף הירידה בפוטנציאל החִנקון (טבלה 2). מחקרים אחרים הראו כי לא רק כמות הגשמים השנתית יכולה להשפיע על מחזור החנקן, אלא גם הדפוס של אירועי הגשמים (עוצמה, כמות ומשך הזמן) יכול לשנות את התוצאות של השלבים השונים במחזור החנקן במערכות אקולוגיות מדבריות [34, 36].
השוני בשכיחות המינים של מחמצני האמוניום (ארכֵאה ובקטריה), בין השנה הראשונה שלאחר תמותת השיחים ובין השנה השנייה (טבלה 2), יכול לנבוע מאסטרטגיות ניצול שונות של האמוניום על-ידי כל אחת משתי קבוצות. נמצא, כי ארכֵאות מסוגלות לנצל ריכוזים נמוכים של אמוניום זמין לגידול [16]. לפיכך, בקרקעות שתכולת המים בהן נמוכה, האמוניום זמין פחות לחמצון, והארכֵאות יכולות להתרבות בקלות רבה יותר מאשר הבקטריות. עם זאת, כאשר תכולת המים בקרקע גדלה, כמו בחורף 2010, האמוניום זמין יותר, והדבר מאפשר שפע גדול יותר של בקטריות (טבלה 2).
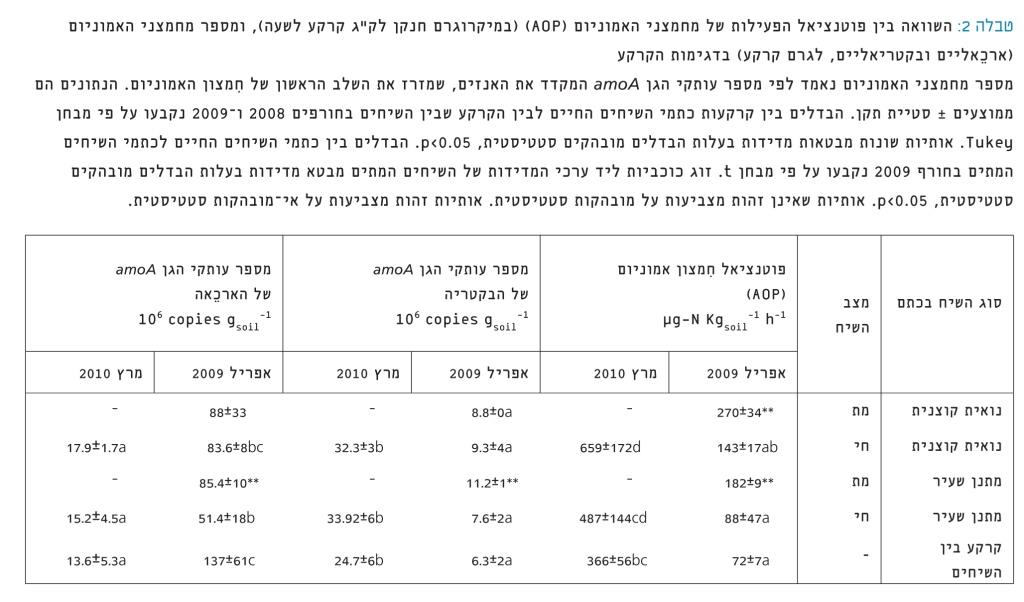
טבלה 2
השוואה בין פוטנציאל הפעילות של מחמצני האמוניום (AOP) (במיקרוגרם חנקן לק"ג קרקע לשעה), ומספר מחמצני האמוניום (ארֵכאליים ובקטריאליים, לגרם קרקע) בדגימות הקרקע
מספר מחמצני האמוניום נאמד לפי מספר עותקי הגן amoA המקדד את האנזים, שמזרז את השלב הראשון של ִחמצון האמוניום. הנתונים הם ממוצעים ± סטיית תקן. הבדלים בין קרקעות כתמי השיחים החיים לבין הקרקע שבין השיחים בחורפים 2008 ו-2009 נקבעו על פי מבחן Tukey. אותיות שונות מבטאות מדידות בעלות הבדלים מובהקים סטטיסטית, 0.05>p. הבדלים בין כתמי השיחים החיים לכתמי השיחים המתים בחורף 2009 נקבעו על פי מבחן t. זוג כוכביות ליד ערכי המדידות של השיחים המתים מבטא מדידות בעלות הבדלים מובהקים סטטיסטית, 0.05>p. אותיות שאינן זהות מצביעות על מובהקות סטטיסטית. אותיות זהות מצביעות על אי-מובהקות סטטיסטית.
כתוצאה מתמותת השיחים נוצר כתם נוסף במערכת, של צמחים מתים, ומאפייני הקרקע שלו שונים מאלה של כתמי שיחים חיים. כתמי שיחים חיים ומתים נבדלו בריכוזי האמוניום בקרקע, ונצפו מגמות שונות בין שני סוגי הכתמים. ריכוזי אמוניום גבוהים נמצאו תחת שיחי נואית קוצנית מתים בהשוואה לאלה החיים, בעוד שריכוזי אמוניום גבוהים נמצאו מתחת לשיחי מתנן שעיר חיים לעומת אלה המתים. תופעה זאת יכולה להיות מוסברת באמצעות התכונות האללופטיות (הפרשה של חומרים שונים אל הסביבה והשפעה על התפתחותם של יצורים אחרים) של המתנן השעיר [15] שיכולות להשפיע ולהפחית פעילויות ביולוגיות מסוימות, כגון פירוק של חומר אורגני וחנקון [5, 12, 15, 22]. כמו כן, יכולות התכונות האללופטיות הללו לתת גם מענה לשכיחות המינים הנמוכה של מחמצני אמוניום שתחת שיחי המתנן השעיר (טבלה 2), בעוד שתחת שיחי הנואית הקוצנית לא נמצאו הבדלים בשכיחות המינים של מחמצני האמוניום.
ממצא חשוב של מחקר זה היה הגילוי כי תחת החופה של שני מיני השיחים המתים, פוטנציאל חמצון האמוניום וריכוזי החנקה היו גבוהים (איור 3). אולם אף על פי שנצפתה פעילות מוגברת של מחמצני אמוניום, לא נמצא שינוי משמעותי בשכיחות המינים. במחקר קודם הצבענו על הבדלים באוכלוסיות החיידקים הכללית בין הכתמים מתחת לחופת הצומח לעומת השטחים שבין הצמחים [5]. ממצאים אלו מצביעים על כך שמחמצני האמוניום רגישים פחות לסוג הכתם ולתנאי יובש. דבר זה נתמך בהצטברות החנקה שהיא תוצאה של פעילות החִנקון בתנאים שנוצרו בעקבות רצף הבצורות.
הירידה בתכולת הרטיבות בקרקע במשך שנות הבצורת בצפון הנגב גורמת לשינויים בדפוסי פעילות המיקרואורגניזמים, הדורשים לחות לפעילותם. דבר זה מביא בעקבותיו להאטת חלק מהמעגלים הביוגאוכימיים (איור 4). עם זאת, יש לציין כי הבצורת פוגעת גם בצמיחת השיחים הצורכים את החנקן. שינויים אלה גורמים להצטברות של חומר אורגני ושל חנקה ואמוניום בעונות היבשות [1, 36]. הצטברות החנקה היא תוצאה של ייצור אמוניום (קיבוע על-ידי מיקרואורגניזמים עמידים ליובש, הפרשות של שבלולים ופירוק של חומר אורגני) וחמצונו לחנקה על-ידי ניטריפיקנטים עמידים ליובש וכן של היעדר הצרכנים (שיחים). תופעות דומות נמצאו גם באזורי מדבר אחרים בעולם [29], אף כי יש לציין כי ייתכן שישנם גורמי אקלים אחרים המעורבים ביצירת תופעות אלה.
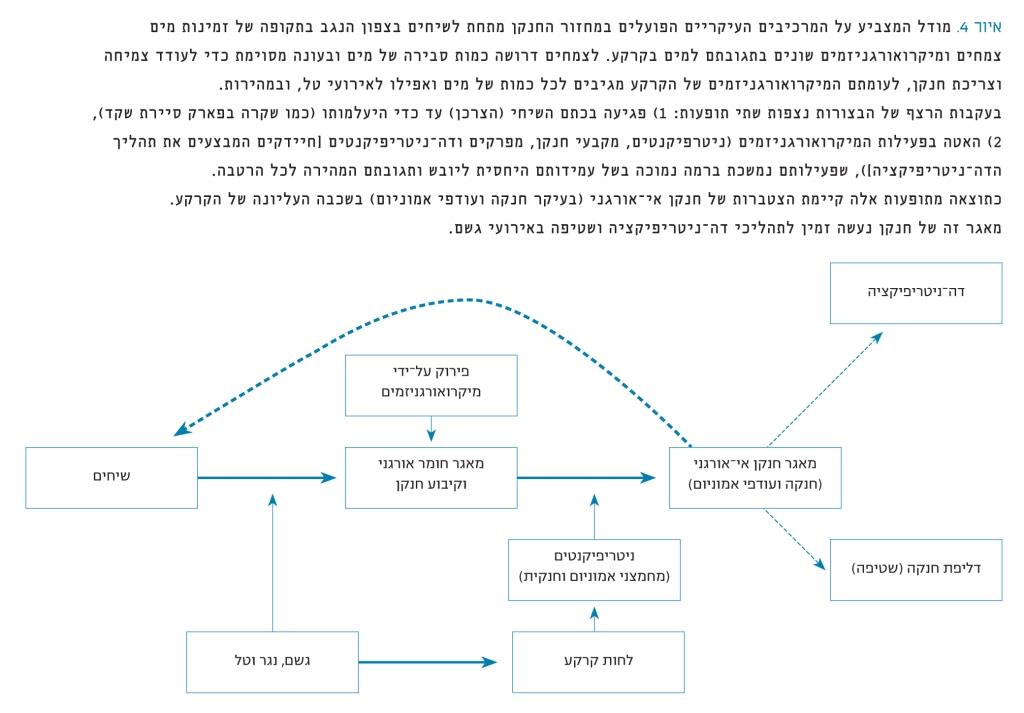
איור 4
מודל המצביע על המרכיבים העיקריים הפועלים במחזור החנקן מתחת לשיחים בצפון הנגב בתקופה של זמינות מים צמחים ומיקרואורגניזמים שונים בתגובתם למים בקרקע
לצמחים דרושה כמות סבירה של מים ובעונה מסוימת כדי לעודד צמיחה וצריכת חנקן, לעומתם המיקרואורגניזמים של הקרקע מגיבים לכל כמות של מים ואפילו לאירועי טל, ובמהירות.
בעקבות הרצף של הבצורות נצפות שתי תופעות: 1) פגיעה בכתם השיחי (הצרכן) עד כדי היעלמותו (כמו שקרה בפארק סיירת שקד), 2) האטה בפעילות המיקרואורגניזמים (ניטרפיקנטים, מקבעי חנקן, מפרקים ודה-ניטריפיקנטים [חיידקים המבצעים את תהליך הדה-ניטריפיקציה]), שפעילותם נמשכת ברמה נמוכה בשל עמידותם היחסית ליובש ותגובתם המהירה לכל הרטבה. כתוצאה מתופעות אלה קיימת הצטברות של חנקן אי-אורגני (בעיקר חנקה ועודפי אמוניום) בשכבה העליונה של הקרקע. מאגר זה של חנקן נעשה זמין לתהליכי דה-ניטריפיקציה ושטיפה באירועי גשם.
נוסף על כך, במחקר זה אנו מציעים כי מיעוט הגשמים הביא להאטה משמעותית בתהליכי הדה-ניטריפיקציה, המעבר של החנקן מתרכובות אורגניות לצורה של אמוניום (ammonification), התנועה של החנקה לעומק הקרקע ובעיקר אי-ניצול החנקה על-ידי השיחים, אלו הסיבות שהביאו להצטברות החנקה והאמוניום בקרקע המדברית. הצטברות החנקה (כאניון –NO3) ברבדים העליונים של הקרקע, בשל היובש, עלולה להוביל לאבדנו במערכת האקולוגית המדברית, שאירועי הגשם בה בתחילת החורף יכולים להיות קיצוניים בעוצמת הגשם ובמשכו (גם בשנים שחונות).
בפארק סיירת שקד אובחן כי באירועים שיורדים בהם יותר מ-10 מ"מ גשם לשעה נוצר נגר עילי המוביל לשיטפון [36]. אירועים כאלה יכולים לשטוף את החנקה מהשכבות העליונות של הקרקע ואף לגרום לתהליכי פריחה של אצות (eutrophication) במאגרי המים במורד. תופעה זו מביאה לאבדן של משאבים יקרים למערכת אקולוגית מדברית שאיננה עשירה בהם, ובעקבותיו לירידה במגוון הביולוגי ובפוריות של המערכת [1]. יש לציין כי שינוי האקלים הגלובלי באזורים צחיחים מאופיין באירועי גשם מעטים אך בעוצמה גבוהה [9]. באירועים כאלה המים העשירים בחנקה מחלחלים לעומק הקרקע ומזהמים את מי התהום [27, 29]. נוסף על כך, היווצרות תנאים אל-אווירניים בפני הקרקע לאחר אירועי גשם תגרום אף לדה-ניטריפיקציה העלולה להיות מלווה בהיווצרות גזי חממה חנקניים [25].

לסיכום, שינוי אקלים, שיכול להתבטא בשנות בצורת רצופות, מאיץ את תהליכי המדבור, והתופעה מתרחשת בעולם וגם בישראל [14]. נוסף על הפגיעה בשירותי המערכת האקולוגית [30] עלולים אזורים אלה גם להפוך למקורות זיהום למים ולאטמוספרה.
תודות
מחקר זה נתמך במענק מחקר מטעם הקרן הישראלית למדע (ISF- 734/05).
סיכום ומשמעויות
המאמר עוסק בתהליכים המתקיימים במערכות אקולוגיות באזורי מדבר בעקבות שנים רצופות של בצורת, ובפרט בשינויים במחזור החנקן בקרקעות צפון הנגב. כל תהליכי החיים בצמח ובקרקע מתרחשים בנוכחות מים ובאמצעותם – בהיעדרם עלול הצמח להיפגע. כמויות מים נמוכות מהרגיל, לאורך מספר שנים רצופות, גורמות ככל הנראה לנזקים מצטברים בשיחים, ובסופו של דבר למותם. גם החנקן הוא מרכיב חשוב בצמח ובהיעדרו מפסיק הצמח לצמוח ולבסוף מת.
במחקר נמצא שכמות החנקה (מקור חנקן זמין לצמחים) תחת שיחי מתנן שעיר שמתו, גבוהה מזו הקיימת תחת שיחי מתנן חיים. עובדה זו מעידה על פעילות של המיקרואורגניזמים האחראים ליצירת החנקה בקרקע, למרות המגבלה בכמות המים. כמות החנקה הגבוהה מתחת לשיחים המתים נובעת ככל הנראה מכמות גדולה יחסית של החנקן הכללי בקרקע, שמקורו בחומר האורגני של השיח המת, ומכך שבמות השיח אין מי שינצל את החנקה. הימשכות הבצורות עשויה לגרום לדעיכת קצב יצירת החנקה בקרקע, בהיעדר אספקת חנקן כללי מהצומח.
משמעויות אפשריות של המחקר הן שבמקרה שרצף הבצורות יימשך או יהיה חלק מתהליך של שינוי האקלים באזור, אזי "עודפי החנקה" יישטפו מהקרקע ויזהמו את מקורות המים. כמו כן, עודפי חנקה עלולים לתרום לזיהום האוויר כתוצאה מתהליך הדה-ניטריפיקציה של החנקה. למסקנות אלו יש להתייחס בזהירות, מכיוון שכמויות החנקה המשתחררות משטחים חקלאיים גדולות הרבה יותר מאלו שהתקבלו במחקר זה, ומשום שמספר שנות בצורת מעידות על תנודות במשקעים באזור ולא על שינוי אקלים המתרחש בטווחי זמן ארוכים מאוד.
המערכת
מקורות
- צעדי א. 1999. מעגל החנקן בכתמיות המדברית. אקולוגיה וסביבה 5: 70–76.
- Adams HD, Guardiola-Claramonte M, Barron-Gafford GA, Villegas JC, Breshears DD, Zou CB, Troch PA, and Huxman TE. 2009. Temperature sensitivity of drought-induced tree mortality portends increased regional die-off under global-change-type drought. Proceedings of the National Academy of Sciences of the United States of America 106: 7063-7066.
- Austin AT, Yahdjian L, Stark JM, Belnap J, Porporato A, Norton U, Ravetta DA, and Schaeffer SM. 2004. Water pulses and biogeochemical cycles in arid and semiarid ecosystems. Oecologia 141: 221-235.
- Beare MH, Coleman DC, Crossley DA, Hendrix PF, and Odum EP. 1995. A hierarchical approach to evaluating the significance of soil biodiversity to biogeochemical cycling. Plant and Soil 170: 5-22.
- Ben-David EA, Zaady E, Sher Y, and Nejidat A. 2011. Assessment of the spatial distribution of soil microbial communities in patchy arid and semi-arid landscapes of the Negev Desert using combined PLFA and DGGE analyses. FEMS Microbiology Ecology 76: 492-503.
- Ben-Dor E and Banin A. 1989. Determination of organic matter content in arid-zone soils using a simple "loss-on-ignition" method. Communications in Soil Science and Plant Analysis 20: 1675-1696.
- Berg N and Steinberger Y. 2008. Role of perennial plants in determining the activity of the microbial community in a Negev Desert ecosystem. Soil Biology and Biochemistry 40: 2686-2695.
- Clesceri LS, Greenberg AE, Eaton AD, and Franson MAH (eds). 1998. Standard methods for the examination of water and wastewater. Washington, DC: American Public Health Association.
- Easterling DR, Meehl GA, Parmesan C, Changnon SA, Karl TR, and Mearns LO. 2000. Climate extremes: Observations, modeling, and impacts. Science 289(5487): 2068-2074.
- Ferree MA and Shannon RD. 2001. Evaluation of a second derivative UV/visible spectroscopy technique for nitrate and total nitrogen analysis of wastewater samples. Water Research 35: 327-332.
- Francis CA, Roberts KJ, Beman JM, Santoro AE, and Oakley BB. 2005. Ubiquity and diversity of ammonia-oxidizing archaea in water columns and sediments of the ocean. Proceedings of the National Academy of Sciences of the United States of America 102: 14683-14688.
- Friedman J. 1987. Allelopathy in desert ecosystems. ACS Symposium Series 330: 53-68.
- Groffman PM and Tiedje JM. 1988. Denitrification hysteresis during wetting and drying cycles in soil. Soil Science Society of America Journal 52: 1626-1629.
- Kalfe HK and Bruins HJ. 2009. Climatic trends in Israel 1970–2002: Warmer and increasing aridity inland. Climatic Change 96: 63-77.
- Ladhari A, Omezzine F, Rinez A, and Haouala R. 2011. Phytotoxicity of Thymelaea hirsute. 3rd International Symposium on Weeds and Invasive Plants; 2–7 Oct 2011; Ascona, Switzerland.
- Martens-Habbena W, Berube PM, Urakawa H, de la Torre JR, and Stahl DA. 2009. Ammonia oxidation kinetics determine niche separation of nitrifying Archaea and Bacteria. Nature 461: 976-979.
- Muyzer G and Smalla K. 1998. Application of denaturing gradient gel electrophoresis (DGGE) and temperature gradient gel electrophoresis (TGGE) in microbial ecology. Antonie Van Leeuwenhoek 73: 127-141.
- Nejidat A. 2005. Nitrification and occurrence of salt-tolerant nitrifying bacteria in the Negev desert soils. FEMS Microbiology Ecology 52: 21-29.
- Perevolotsky A and Seligman NG. 1998. Role of grazing in Mediterranean rangeland ecosystems. BioScience 48: 1007-1017.
- Reynolds JF, Stafford-Smith DM, Lambin EF, Turner II BL, Mortimore M, Batterbury SPJ, Downing TE, Dowlatabadi H, Fernández RJ, Herrick JE, Huber-Sannwald E, Jiang H, Leemans R, Lynam T, Maestre FT, Ayarza M, and Walker B. 2007. Global desertification: Building a science for dryland development. Science 316: 847-851.
- Rotthauwe J, Witzel K, and Liesack W. 1997. The ammonia mono-oxygenase structural gene amoA as a functional marker: Molecular fine-scale analysis of natural ammonia-oxidizing populations. Applied and Environmental Microbiology 63: 4704-4712.
- Saul-Tcherkas V and Steinberger Y. 2009. Temporal and shrub adaptation effect on soil microbial functional diversity in a desert system. European Journal of Soil Science 60: 871-882.
- Schlesinger WH and Pilmanis AM. 1998. Plant-soil interactions in deserts. Biogeochemistry 42: 169-187.
- Smith CJ and Osborn AM. 2009. Advantages and limitations of quantitative PCR (Q-PCR)-based approaches in microbial ecology. FEMS Microbiology Ecology 67: 6-20.
- Smith K. 1997. The potential for feedback effects induced by global warming on emissions of nitrous oxide by soils. Global Change Biology 3: 327-338.
- van der Putten WH, Anderson JM, Bardgett RD, Behan-Pelletier V, Bignell DE, Brown GG, Brown VK, Brussaard L, Hunt HW, Ineson P, Jones TH, Lavelle P, Paul EA, St. John M, Wardle DA, Wojtowicz T, and Wall DH. 2004. The sustainable delivery of goods and services provided by soil biota. In: Wall DH (Ed). Sustaining biodiversity and ecosystem services in soils and sediments. SCOPE 64. Washington DC: Island Press.
- Veluci RM, Neher DA, and Weicht TR. 2006. Nitrogen fixation and leaching of biological soil crust communities in mesic temperate soils. Microbial Ecology 51: 189-196.
- Walther GR, Post E, Convey P, Menzel A, Parmesan C, Beebee TJC, Fromentin JM, Hoegh-Guldberg O, and Bairlein F. 2002. Ecological responses to recent climate change. Nature 416: 389-395.
- Walvoord MA, Phillips FM, Stonestrom DA, Evans RD, Hartsough PC, Newman BD, and Striegl RG. 2003. A reservoir of nitrate beneath desert soils. Science 302: 1021-1024.
- Wardle DA, Brown VK, Behan-Pelletier V, St. John M, Wojtowicz T, Bardgett RD, Brown GG, Ineson P, Lavelle P, van der Putten WH, Anderson JM, Brussaard L, Hunt HW, Paul EA, and Wall DH. 2004. Vulnerability to global change of ecosystem goods and services driven by soil biota. In: Wall DH (Ed). Sustaining biodiversity and ecosystem services in soils and sediments. SCOPE 64. Washington DC: Island Press.
- West NE. 1991. Nutrient cycling in soils of semiarid and arid regions. In: Skujins J (Ed). Semiarid lands and deserts: Soil resource and reclamation. New York: Marcel Dekker.
- Whitford W. 2002. Ecology of desert systems. London: Academic Press.
- Yahdjian L, Gherardi L, and Sala OE. 2011. Nitrogen limitation in arid-subhumid ecosystems: A meta-analysis of fertilization studies. Journal of Arid Environments 75: 675-680.
- Yahdjian L and Sala OE. 2010. Size of precipitation pulses controls nitrogen transformation and losses in an arid Patagonian ecosystem. Ecosystems 13: 575-585.
- Young IM, Blanchart E, Chenu C, Dangerfiled M, Fragoso C, Grimaldi M, Ingram J, and Monrozier LJ. 1998. The interaction of soil biota and soil structure under global change. Global Change Biology 4: 703-712.
- Zaady E. 2005. Seasonal changes and nitrogen cycling in a patchy Negev desert, a review. Arid Land Research and Management 19: 111-124.
- Zaady E, Groffman PM, and Shachak M. 1996. Litter as a regulator of N and C dynamics in macrophytic patches in Negev desert soils. Soil Biology and Biochemistry 28: 39-46.






 מהדורה מודפסת
מהדורה מודפסת












